Adénosylméthionine décarboxylase
Adénosylméthionine décarboxylase
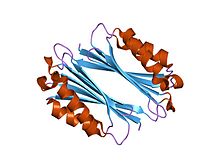
Structure d'une adénosylméthionine décarboxylase cristallisée de Thermotoga maritima (PDB 1TLU[1])
| N° EC | EC 4.1.1.50 |
|---|---|
| N° CAS | 9036-20-8 |
| Cofacteur(s) | pyruvate |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
modifier 
L'adénosylméthionine décarboxylase est une lyase qui catalyse la réaction :
- S-adénosyl-L-méthionine S-adénosylméthioninamine + CO2.
Cette enzyme intervient dans la biosynthèse de polyamines naturelles telles que la spermidine et la spermine[2]. Elle a pour cofacteur le pyruvate et non le phosphate de pyridoxal[3].
Notes et références
- ↑ (en) Angela V. Toms, Cynthia Kinsland, Diane E. McCloskey, Anthony E. Pegg et Steven E. Ealick, « Evolutionary Links as Revealed by the Structure of Thermotoga maritima S-Adenosylmethionine Decarboxylase », Journal of Biological Chemistry, vol. 279, no 32, , p. 33837-33846 (PMID 15150268, DOI 10.1074/jbc.M403369200, lire en ligne)
- ↑ (en) A. E. Pegg, H. Xiong, D. J. Feith et L. M. Shantz, « S-adenosylmethionine decarboxylase: structure, function and regulation by polyamines », Biochemical Society Transactions, vol. 26, no 4, , p. 580-586 (PMID 10047786)
- ↑ (en) Paul D. van Poelje et Esmond E. Snell, « Pyruvoyl-Dependent Enzymes », Annual Review of Biochemistry, vol. 59, , p. 29-59 (PMID 2197977, DOI 10.1146/annurev.bi.59.070190.000333, lire en ligne)
 Portail de la biochimie
Portail de la biochimie











