Percarbonate de sodium
| Percarbonate de sodium | |||
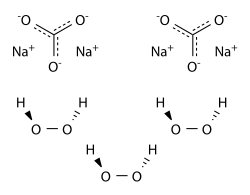 | |||
| Constituants du percarbonate de sodium | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | percarbonate de sodium | ||
| Synonymes | peroxhydrate de carbonate de sodium, carbonate de sodium peroxyhydraté | ||
| No CAS | 15630-89-4 | ||
| No ECHA | 100.036.082 | ||
| No CE | 239-707-6 | ||
| PubChem | 159762 | ||
| SMILES | C(=O)([O-])[O-].C(=O)([O-])[O-].OO.OO.OO.[Na+].[Na+].[Na+].[Na+] PubChem, vue 3D | ||
| InChI | Std. InChI : vue 3D InChI=1S/2CH2O3.4Na.3H2O2/c2*2-1(3)4;;;;;3*1-2/h2*(H2,2,3,4);;;;;3*1-2H/q;;4*+1;;;/p-4 Std. InChIKey : MSLRPWGRFCKNIZ-UHFFFAOYSA-J | ||
| Apparence | Solide incolore cristallisé hygroscopique | ||
| Propriétés chimiques | |||
| Formule | C2H6Na4O122 Na2CO3·3 H2O2 | ||
| Masse molaire[1] | 314,020 9 ± 0,005 6 g/mol C 7,65 %, H 1,93 %, Na 29,28 %, O 61,14 %, | ||
| Précautions | |||
| SGH[2] | |||
   Danger H272 : Peut aggraver un incendie ; comburant H302 : Nocif en cas d'ingestion H318 : Provoque des lésions oculaires graves P220 : Tenir/stocker à l’écart des vêtements/…/matières combustibles P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P305 : En cas de contact avec les yeux : P338 : Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P351 : Rincer avec précaution à l’eau pendant plusieurs minutes. | |||
| Transport[3] | |||
Code Kemler : 50 : matière comburante (favorise l'incendie) Numéro ONU : 3378 : CARBONATE DE SODIUM PEROXYHYDRATÉ Classe : 5.1 Étiquette :  5.1 : Matières comburantes Emballage : Groupe d'emballage II/III : matières moyennement/faiblement dangereuses. | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
Le percarbonate de sodium, parfois appelé peroxhydrate de carbonate de sodium, carbonate de sodium peroxyhydraté ou percarbonate de soude, est un composé chimique de formule 2Na2CO3·3H2O2.
Propriétés et chimie de base
Le percarbonate de sodium se présente sous la forme d'un solide cristallisé incolore et hygroscopique, soluble dans l'eau en donnant une solution très basique. Il résulte de l'addition de peroxyde d'hydrogène H2O2 à du carbonate de sodium Na2CO3 :
- 2 Na2CO3 + 3 H2O2 → 2Na2CO3·3H2O2.
Une fois dissous dans l'eau, il se décompose en ses constituants :
- carbonate de sodium ou « cristaux de soude », substances apportant un pH aux alentours de 9-10.
- peroxyde d'hydrogène, agent de blanchiment à « l'oxygène actif ».
Toxicité
S’il n'est pas toxique pour l'environnement, le percarbonate de sodium peut être irritant. De plus, tout en étant non combustible, il peut toutefois favoriser la combustion d’autres substances[4].
Utilisation
Il est utilisé dans certains produits de blanchiment à la place du perborate de sodium Na2B2O4(OH)4, ainsi qu'en laboratoire pour produire du peroxyde d'hydrogène anhydre.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ SIGMA-ALDRICH
- ↑ a et b Entrée « Sodium carbonate peroxohydrate » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 24 avril 2011 (JavaScript nécessaire)
- ↑ Organisation internationale du travail, « ICSC 1744 - PERCARBONATE DE SODIUM, ILO (fiche) », sur ilo.org/, (consulté le )
v · m | |
|---|---|
|
 Portail de la chimie
Portail de la chimie











