Sorbitol déshydrogénase
Sorbitol déshydrogénase
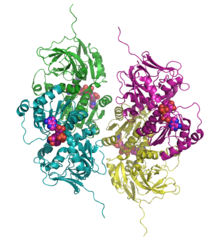
Sorbitol déshydrogénase humaine complexée avec le NAD+ (PDB 1PL8[1])
| N° EC | EC 1.1.1.14 |
|---|---|
| N° CAS | 9028-21-1 |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
modifier 
La sorbitol déshydrogénase (SDH), ou L-iditol 2-déshydrogénase, est une oxydoréductase qui catalyse la réaction :
- L-iditol + NAD+ L-sorbose + NADH + H+.
Cette enzyme est très largement distribuée chez les êtres vivants et a été retrouvée chez les archées, les bactéries, les levures, les plantes et les animaux. Elle agit sur un grand nombre d'alditols, notamment sur le L-iditol, le D-glucitol, le D-xylitol et le D-galactitol. Des enzymes de tissus différents auront des spécificités différentes vis-à-vis des substrats. Cette enzyme est spécifique du NAD+ et ne fonctionne pas avec le NADP+. Un cation de zinc intervient également dans la catalyse.
Elle est connue notamment pour convertir le sorbitol, issu du glucose, en fructose[2] :

Notes et références
 Portail de la biochimie
Portail de la biochimie











