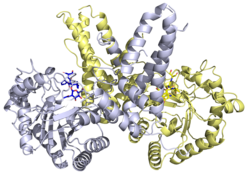
| MGEA5 |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| |
| Ідентифікатори |
|---|
| Символи | OGA, MEA5, NCOAT, meningioma expressed antigen 5 (hyaluronidase), MGEA5, O-GlcNAcase |
|---|
| Зовнішні ІД | OMIM: 604039 MGI: 1932139 HomoloGene: 8154 GeneCards: OGA |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • hyalurononglucosaminidase activity
• beta-N-acetylglucosaminidase activity
• hydrolase activity
• hydrolase activity, acting on glycosyl bonds
• [protein-3-O-(N-acetyl-D-glucosaminyl)-L-threonine O-N-acetyl-alpha-D-glucosaminase activity]
• [protein-3-O-(N-acetyl-D-glucosaminyl)-L-serine O-N-acetyl-alpha-D-glucosaminase activity]
• [protein-3-O-(N-acetyl-D-glucosaminyl)-L-serine/L-threonine O-N-acetyl-alpha-D-glucosaminase activity]
|
|---|
| Клітинна компонента | • цитоплазма
• гіалоплазма
• мембрана
• клітинне ядро
|
|---|
| Біологічний процес | • обмін речовин
• protein deglycosylation
• N-acetylglucosamine metabolic process
• glycoprotein catabolic process
• protein O-linked glycosylation
• glycoprotein metabolic process
• GO:0022415 viral process
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
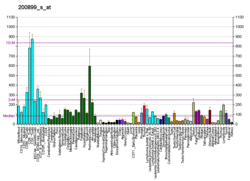
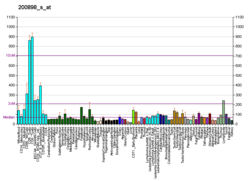 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | |
|---|
| RefSeq (білок) | | |
|---|
| Локус (UCSC) | Хр. 10: 101.78 – 101.82 Mb | Хр. 19: 45.74 – 45.77 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
MGEA5 (англ. Meningioma expressed antigen 5 (hyaluronidase)) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 10-ї хромосоми.[3] Довжина поліпептидного ланцюга білка становить 916 амінокислот, а молекулярна маса — 102 915[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MVQKESQATL | | EERESELSSN | | PAASAGASLE | | PPAAPAPGED | | NPAGAGGAAV |
| AGAAGGARRF | | LCGVVEGFYG | | RPWVMEQRKE | | LFRRLQKWEL | | NTYLYAPKDD |
| YKHRMFWREM | | YSVEEAEQLM | | TLISAAREYE | | IEFIYAISPG | | LDITFSNPKE |
| VSTLKRKLDQ | | VSQFGCRSFA | | LLFDDIDHNM | | CAADKEVFSS | | FAHAQVSITN |
| EIYQYLGEPE | | TFLFCPTEYC | | GTFCYPNVSQ | | SPYLRTVGEK | | LLPGIEVLWT |
| GPKVVSKEIP | | VESIEEVSKI | | IKRAPVIWDN | | IHANDYDQKR | | LFLGPYKGRS |
| TELIPRLKGV | | LTNPNCEFEA | | NYVAIHTLAT | | WYKSNMNGVR | | KDVVMTDSED |
| STVSIQIKLE | | NEGSDEDIET | | DVLYSPQMAL | | KLALTEWLQE | | FGVPHQYSSR |
| QVAHSGAKAS | | VVDGTPLVAA | | PSLNATTVVT | | TVYQEPIMSQ | | GAALSGEPTT |
| LTKEEEKKQP | | DEEPMDMVVE | | KQEETDHKND | | NQILSEIVEA | | KMAEELKPMD |
| TDKESIAESK | | SPEMSMQEDC | | ISDIAPMQTD | | EQTNKEQFVP | | GPNEKPLYTA |
| EPVTLEDLQL | | LADLFYLPYE | | HGPKGAQMLR | | EFQWLRANSS | | VVSVNCKGKD |
| SEKIEEWRSR | | AAKFEEMCGL | | VMGMFTRLSN | | CANRTILYDM | | YSYVWDIKSI |
| MSMVKSFVQW | | LGCRSHSSAQ | | FLIGDQEPWA | | FRGGLAGEFQ | | RLLPIDGAND |
| LFFQPPPLTP | | TSKVYTIRPY | | FPKDEASVYK | | ICREMYDDGV | | GLPFQSQPDL |
| IGDKLVGGLL | | SLSLDYCFVL | | EDEDGICGYA | | LGTVDVTPFI | | KKCKISWIPF |
| MQEKYTKPNG | | DKELSEAEKI | | MLSFHEEQEV | | LPETFLANFP | | SLIKMDIHKK |
| VTDPSVAKSM | | MACLLSSLKA | | NGSRGAFCEV | | RPDDKRILEF | | YSKLGCFEIA |
| KMEGFPKDVV | | ILGRSL |
Кодований геном білок за функціями належить до гідролаз, глікозидаз, фосфопротеїнів. Задіяний у такому біологічному процесі, як альтернативний сплайсинг. Локалізований у цитоплазмі, ядрі.
Література
- Comtesse N., Maldener E., Meese E. (2001). Identification of a nuclear variant of MGEA5, a cytoplasmic hyaluronidase and a beta-N-acetylglucosaminidase. Biochem. Biophys. Res. Commun. 283: 634—640. PMID 11341771 DOI:10.1006/bbrc.2001.4815
- Gao Y., Wells L., Comer F.I., Parker G.J., Hart G.W. (2001). Dynamic O-glycosylation of nuclear and cytosolic proteins: cloning and characterization of a neutral, cytosolic beta-N-acetylglucosaminidase from human brain. J. Biol. Chem. 276: 9838—9845. PMID 11148210 DOI:10.1074/jbc.M010420200
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Cetinbas N., Macauley M.S., Stubbs K.A., Drapala R., Vocadlo D.J. (2006). Identification of Asp174 and Asp175 as the key catalytic residues of human O-GlcNAcase by functional analysis of site-directed mutants. Biochemistry. 45: 3835—3844. PMID 16533067 DOI:10.1021/bi052370b
- Schimpl M., Schuttelkopf A.W., Borodkin V.S., van Aalten D.M. (2010). Human OGA binds substrates in a conserved peptide recognition groove. Biochem. J. 432: 1—7. PMID 20863279 DOI:10.1042/BJ20101338
- Schimpl M., Borodkin V.S., Gray L.J., van Aalten D.M. (2012). Synergy of peptide and sugar in O-GlcNAcase substrate recognition. Chem. Biol. 19: 173—178. PMID 22365600 DOI:10.1016/j.chembiol.2012.01.011
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:7056 (англ.) . Процитовано 8 вересня 2017.
{{cite web}}: Обслуговування CS1: Сторінки з параметром url-status, але без параметра archive-url (посилання) - ↑ UniProt, O60502 (англ.) . Архів оригіналу за 25 серпня 2017. Процитовано 8 вересня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|















