Acénaphtène
| Acénaphtène | |||
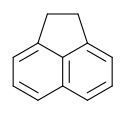  Structure de l'acénaphtène. | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | 1,2-dihydroacénaphthylène | ||
| Synonymes | 1,8-éthylènenaphthalène | ||
| No CAS | 83-32-9 | ||
| No ECHA | 100.001.336 | ||
| No CE | 201-469-6 | ||
| No RTECS | AB1000000 | ||
| PubChem | 6734 | ||
| SMILES | c2cc1cccc3c1c(c2)CC3 PubChem, vue 3D | ||
| InChI | InChI : vue 3D InChI=1/C12H10/c1-3-9-4-2-6-11-8-7-10(5-1)12(9)11/h1-6H,7-8H2 | ||
| Apparence | Poudre cristalline blanche à jaune | ||
| Propriétés chimiques | |||
| Formule | C12H10 [Isomères] | ||
| Masse molaire[2] | 154,207 8 ± 0,010 3 g/mol C 93,46 %, H 6,54 %, | ||
| Susceptibilité magnétique | 109,3×10-6 cm3·mol-1[1] | ||
| Propriétés physiques | |||
| T° fusion | 93,4 °C [3] | ||
| T° ébullition | 279 °C [3] | ||
| Solubilité | 3,9 mg·l-1 (eau,25 °C)[4] 36,52 mg·g-1 (éthanol,25,05 °C) 31,10 mg·g-1 (propan-2-ol,24,92 °C) 50,40 mg·g-1 (butan-1-ol,25,1 °C) 401,70 mg·g-1 (toluène,25,08 °C)[5] | ||
| Masse volumique | 1,222 g·cm-3 à 20 °C [3] | ||
| T° d'auto-inflammation | 450 °C [6] | ||
| Point d’éclair | 135 °C [6] | ||
| Thermochimie | |||
| S0solide | 188,87 J·K-1·mol-1 [7] | ||
| ΔfH0gaz | 156,8 kJ·mol-1 [7] | ||
| ΔfH0solide | 72 kJ·mol-1 [7] | ||
| ΔfusH° | 21,462 2 kJ·mol-1 à 93,41 °C [7] | ||
| ΔvapH° | 63,9 kJ·mol-1 à 25 °C [8] | ||
| Cp | 185,27 J·K-1·mol-1 (solide,17,15 °C) [9] 220,85 J·K-1·mol-1 (gaz,126,85 °C)[7] | ||
| PCI | −6 222 kJ·mol-1 [7] | ||
| Propriétés optiques | |||
| Indice de réfraction | [3] | ||
| Précautions | |||
| SGH[10] | |||
  Attention H315 : Provoque une irritation cutanée H319 : Provoque une sévère irritation des yeux H335 : Peut irriter les voies respiratoires H410 : Très toxique pour les organismes aquatiques, entraîne des effets à long terme P261 : Éviter de respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols. P273 : Éviter le rejet dans l’environnement. P305 : En cas de contact avec les yeux : P338 : Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P351 : Rincer avec précaution à l’eau pendant plusieurs minutes. P501 : Éliminer le contenu/récipient dans … | |||
| NFPA 704 | |||
1 2 1 | |||
| Transport[6] | |||
Code Kemler : 90 : matière dangereuse du point de vue de l'environnement, matières dangereuses diverses Numéro ONU : 3077 : MATIÈRE DANGEREUSE DU POINT DE VUE DE L’ENVIRONNEMENT, SOLIDE, N.S.A. Classe : 9 Étiquettes :  9 : Matières et objets dangereux divers  9.1 Emballage : Groupe d'emballage III : matières faiblement dangereuses. | |||
| Écotoxicologie | |||
| CL50 | 600 mg·kg-1 (rat, i.p.) [4] | ||
| LogP | 3,92 [6] | ||
| Composés apparentés | |||
| Isomère(s) | Acénaphtylène | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
L'acénaphtène est un hydrocarbure aromatique polycyclique (HAP) constitué d'une molécule de naphtalène dont les carbones 1 et 8 sont reliés par un pont éthylénique. C'est la forme hydrogénée de l'acénaphtylène.
C'est un constituant du goudron, et on le trouve aussi dans la houille ainsi qu'en très faible quantité dans le pétrole.
Histoire
L'acénaphthène a été découvert pour la première fois par Marcellin Berthelot dans le goudron en 1867[11], puis synthétisée ensuite avec Bardy à partir de l'α-éthylnaphthalène.
Propriétés physico-chimiques
L'acénaphtène est presque insoluble dans l'eau, mais est en revanche soluble dans le benzène, l'éther, le chloroforme et dans l'alcool à chaud.
Cet hydrocarbure réagit avec les halogènes de manière préférentielle en position 3, 5 et 6 voire 1 en fonction de l'activation. La nitration et la sulfonation ont lieu également sur ces positions.
L'hydrogénation catylique conduit à la formation du tétrahydroacénaphtène et du décahydroacénaphtène alors que l'oxydation donne l'acénaphtylène, l'acide naphtalique, l'anhydride naphtalique, l'acénaphtènequinone, l'acénaphténol et l'acénaphténone[11].
Utilisation
L'acénaphtène est produit en grande quantité pour la synthèse de l'anhydride naphtalique par oxydation en phase gazeuse. L'oxydation a lieu en présence d'air et d'un catalyseur à base de vanadium à 300–400 °C[11]. L'acide naphtalique est produit par oxydation en phase liquide en présence de chromate ou d'air accompagné d'acétate de manganèse voire d'acétate de cobalt aux environs de 200 °C[11]. La condensation avec le propanédinitrile donne l'acide naphtalèn-1,4,5,8-tétracarboxylique. Ces composés sont des intermédiaires pour la fabrication de pigments pérylènes et périnones[11].
D'autres intermédiaires pour la fabrication de colorants ou de produits pharmaceutiques utilisent l'acénaphtène comme réactif: le 4-bromacénaphtène pour la production d'anhydride 4-bromonaphtalique, le 5,6-dichloracénaphtène et le 3,5,6-trichloracénaphtène. Le pigment fluorescent Solvent yellow 44 est fabriqué via l'anhydride 4-nitronaphtalique qui est le résultat de la nitration et de l'oxydation de l'acénaphtène[11].
Des plastiques thermiquement stables ou non-inflammables par incorporation de dérivés de l'acénaphtène durant la polymérisation[11].
Production et synthèse
Le goudron contient environ 0,3 % d'acénaphtène et 2 % d'acénaphtylène qui peut être converti via hydrogénation. L'acénaphtène est concentrée dans la fraction du goudron ayant un point d'ébullition compris entre 230 et 290 °C jusqu'à 25 %. Une seconde distillation est effectuée pour obtenir une solution concentrée ayant un point d'ébullition entre 270 et 275 °C suivie d'une cristallisation pour l'obtention de l'acénaphtène technique (95-99 %)[11]. Une suite de distillation et recristallisation permet une meilleure purification du produit[11].
Voir aussi
Liens externes
- (en) Method for sampling and analysis (méthode d'échantillonnage et d'analyse)
- (en) Chemical land datasheet
- (en) MSDS at Oxford University Page de l'université d'Oxford)
- (en) National Pollutant Inventory - Polycyclic Aromatic Hydrocarbon Fact Sheet
- (en) Entrée « Acénaphtène » de la base d'une base de données HAP
Références
- ↑ (en) Hyp J. Dauben, Jr., James D. Wilson et John L. Laity, « Diamagnetic Susceptibility Exaltation in Hydrocarbons », Journal of the American Chemical Society, vol. 91, no 8, , p. 1991-1998
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a b c et d (en) W. M Haynes, CRC Handbook of chemistry and physics, Boca Raton, CRC Press/Taylor and Francis, , 91e éd., 2610 p. (ISBN 978-143982-077-3), p. 3-4
- ↑ a et b (en) « Acénaphtène », sur ChemIDplus, consulté le 18 janvier 2010
- ↑ (en) Fang He et Pengbiao Liu, « Solubility of Acenaphthylene in Different Solvents between (278 and 323) K », Journal of Chemical & Engineering Data, vol. 52, no 6, , p. 2536-2537
- ↑ a b c d et e Entrée « Acenaphthene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 18 janvier 2010 (JavaScript nécessaire)
- ↑ a b c d e et f (en) « Acenaphthene », sur NIST/WebBook, consulté le 18 janvier 2010
- ↑ (en) Ying Duan Lei, Raymond Chankalal, Anita Chan et Frank Wania, « Supercooled Liquid Vapor Pressures of the Polycyclic Aromatic Hydrocarbons », Journal of Chemical & Engineering Data, vol. 47, no 4, , p. 801-806
- ↑ (en) J. A. R. Cheda et E. F. Jr. Westrum, « Subambient-Temperature Thermophysics of Acenaphthene and Acenaphthylene: Molecular Disorder in the Latter », The Journal of Physical Chemistry, vol. 98, no 9, , p. 2482-2488
- ↑ SIGMA-ALDRICH
- ↑ a b c d e f g h et i (en) Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke, Hydrocarbons, Wiley-VCH Verlag GmbH & Co, coll. « Ullmann's Encyclopedia of Industrial Chemistry »,
v · m | |
|---|---|
| 2 cycles | |
| 3 cycles |
|
| 4 cycles |
|
| 5 cycles |
|
| 6 cycles et plus |
|
 Portail de la chimie
Portail de la chimie













