Fosfofruktokinaza
| Fosfofruktokinaza | |||||
|---|---|---|---|---|---|
| Identifikatori | |||||
| Simbol | Ppfruckinase | ||||
| Pfam | PF00365 | ||||
| InterPro | IPR000023 | ||||
| PROSITE | PDOC00336 | ||||
| |||||
Fosfofruktokinaza je kinazni enzim koji fosforilizuje fruktozu 6-fosfat tokom glikolize.
Enzimski katalizovani transfer fosforil grupe sa ATP je važna reakcija u mnoštvu raznovrsnih bioloških procesa.[1] Jedan od enzima koji koriste tu reakciju je fosfofruktokinaza (PFK), koja katalizuje fosforilaciju fruktoza-6-fosfata do fruktoza-1,6- bisfosfata, što je ključni regulatorni korak u glikolitičkom putu.[2][3] PFK se javlja kao homotetramer kod bacterija i sisara (pri čemu svaki monomer poseduje 2 slična domena) i kao oktomer kod kvasca (gde postoje 4 alfa- (PFK1) i 4 beta-lanca (PFK2), oni poput monomera sisara poseduju 2 slična domena[3]). Ovaj protein može da koristi morfeinski model alosterne regulacije.[4]
Postoje dva tipa ovog enzima:
| Tip | Sinonimi | EC broj | Supstrat | Produkt | Podjedinični geni |
|---|---|---|---|---|---|
| Fosfofruktokinaza 1 | 6-fosfofruktokinaza fosfoheksokinaza | EC 2.7.1.11 |  Fruktoza 6-fosfat |  Fruktoza-1,6-bisfosfat | PFKL, PFKM, PFKP |
| Fosfofruktokinaza 2 | 6-fosfofrukto-2-kinaza | EC 2.7.1.105 | 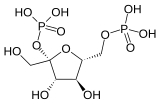 Fruktoza 2,6-bisfosfat | PFKFB1, PFKFB2, PFKFB3, PFKFB4 |
Povezano
- Fosfofruktokinazna deficijencija
Reference
- ↑ Evans PR, Hellinga HW (1987). „Mutations in the active site of Escherichia coli phosphofructokinase”. Nature 327 (6121): 437–439. DOI:10.1038/327437a0. PMID 2953977.
- ↑ Wegener G, Krause U (2002). „Different modes of activating phosphofructokinase, a key regulatory enzyme of glycolysis, in working vertebrate muscle”. Biochem. Soc. Trans. 30 (2): 264–270. DOI:10.1042/bst0300264. PMID 12023862.
- ↑ 3,0 3,1 Raben N, Exelbert R, Spiegel R, Sherman JB, Nakajima H, Plotz P, Heinisch J (1995). „Functional expression of human mutant phosphofructokinase in yeast: genetic defects in French Canadian and Swiss patients with phosphofructokinase deficiency”. Am. J. Hum. Genet. 56 (1): 131–141. PMC 1801305. PMID 7825568.
- ↑ T. Selwood and E. K. Jaffe. (2011). „Dynamic dissociating homo-oligomers and the control of protein function.”. Arch. Biochem. Biophys. 519 (2): 131–43. DOI:10.1016/j.abb.2011.11.020. PMC 3298769. PMID 22182754.
Vanjske veze
- MeSH Phosphofructokinases
- p
- r
- u
fosfotransferaze/kinaze
(PO4)
2.7.1: OH- akceptor | Hekso- • Gluko- • Frukto- (Hepatička) • Galakto- • Fosfofrukto- (1, Jetra, Mišić, Trombocit, 2) • Riboflavin • Šikimat • Timidin (ADP-timidin) • NAD+ • Glicerol • Pantotenat • Mevalonat • Piruvat • Deoksicitidin • PFP • Diacilglocerol • Fosfoinozitid 3 (Klasa I PI 3, Klasa II PI 3) • Sfingozin • Glukoza-1,6-bisfosfat sintaza |
|---|---|
2.7.2: COOH akceptor | |
2.7.3: N akceptor | |
2.7.4: PO4 akceptor |
(P2O7)
(PO4-nukleozid)
| |||||
Druge |
Fosfatidiltransferaze | |
|---|---|
Glikozil-1-fosfotransferaza |
(PO4; proteinski akceptor)
2.7.10: proteinske-tirozinske | vidi tirozinske kinaze |
|---|---|
2.7.11: proteinske-serin/treonin | vidi serin/treonin-specifične proteinske kinaze |
2.7.12: dualna specifičnost | vidi serin/treonin-specifične proteinske kinaze |
2.7.13: protein-histidinske |









